近日,我室韩克利研究员团队基于氨基甲酸酯母核的结构与功能关系,设计并发展了小分子抑制剂型荧光探针(SMI-probe),在重要的药物代谢酶羧酸酯酶(Carboxylesterases,CEs)的实时荧光高分辨检测中取得了良好的应用效果。由于抑制剂型探针分子NIC-4的分子结构简单,体积小,且具有针对CEs的超分辨响应灵敏度,因此在细胞原位检测中能够获得更加真实的成像效果,为亚细胞器层面的酶标记提供了新的设计思路与成功范例。
羧酸酯酶CEs是一类重要的水解酶,在外源性药物代谢过程中,其负责催化的酯水解过程,是包括伊立替康等在内的抗癌药物起效的关键激活步骤。此外,CEs在维持内源性脂质和糖代谢稳定中发挥着十分重要的作用。对CEs的原位实时荧光标记,是实现糖/脂代谢平衡深入理论研究及抗肿瘤药物应用效果监测的实践基础。传统的免疫荧光标记策略能够标记CE,但该方法操作复杂,依靠免疫级联反应实现的信号放大对所应用的抗体质量有非常高的要求,标记抗体结构过大会导致成像失真,且只能用于固定细胞,无法实现实时在体成像。
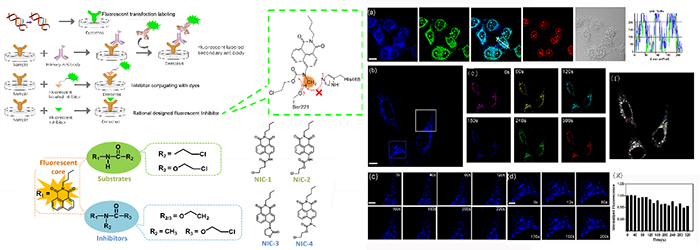
利用荧光核偶联识别基团是超分辨探针设计的一大策略,目前已有纳米颗粒(Nanobodies),适体(Aptamers)荧光标记等策略。基于轻便且具有高选择性标记的超分辨荧光探针的应用需求,韩克利团队在被标记蛋白配体属性的结构功能研究的基础上,结合数据分析与挖掘,发现氨基甲酸酯类化合物在羧酸酯酶催化识别上具有显著的分型特点,即具有R1-NH-CO-R2型结构特点的氨基甲酸酯类化合物趋向于成为可被羧酸酯酶催化代谢的底物,而R1-NR2-CO-R3型则易成为羧酸酯酶的抑制剂化合物。基于此,团队选择结构较小的荧光基团萘酰亚胺,将抑制剂结构基础与荧光母核进行直接连接,设计得到小分子抑制剂型荧光探针NIC-4,通过理论计算确认,其抑制性质来源于酰胺键中较大空间位阻的取代基对酶活性中心丝氨酸亲核进攻过程的阻碍。进一步通过抑制属性检测、荧光属性标定、标记选择性验证等,团队确认了探针小分子的优良体外属性,并在细胞层面对亚细胞器的实时荧光标记表现进行了验证,结果显示,设计得到的超分辨荧光探针小分子不仅在标记选择性上优于免疫荧光方法,也具有良好的细胞耐受性(低细胞毒)、高检测灵敏度、荧光稳定性等,应用其进行长时间的细胞动态效应观测,具有显著优势。
相关成果以“Directional Modified Fluorophores for Super Resolution Imaging of Target Enzymes: A Case study with Carboxylesterases”为题,发表在《药物化学》(Journal of Medicinal Chemistry)杂志上。该工作的第一作者是我室贾燕助理研究员和北京大学深圳医院博士后王家悦。该工作得到国家自然科学基金、博士后面上基金等项目的资助。(文/图 王家悦、贾燕)
文章链接:https://doi.org/10.1021/acs.jmedchem.1c01469